Qu’ont en commun le virus SARS-CoV-2, les libellules, et les hommes ? Tous se reproduisent… et meurent. Pour comprendre ces cycles de vie particulièrement diversifiés, différents modèles mathématiques ont été développés depuis le XVIIIe siècle : comment les populations croissent et décroissent selon les conditions environnementales, parviennent à subsister malgré les fluctuations de leurs conditions de vie, etc.
Ces modèles d’étude des populations peuvent aussi être utilisés par les épidémiologistes pour comprendre comment les virus émergent et se propagent. Jusque-là largement méconnus du grand public, ils se sont retrouvés sur le devant de la scène médiatique lors des premiers mois de l’épidémie de Covid-19 début 2020, du fait de leur rôle crucial pour guider les politiques de santé publique. Car ils peuvent être appliqués au SARS-CoV-2, tant à ses premières versions qu’à ses variants préoccupants successifs Alpha, Delta ou Omicron…
Une particularité des variants est qu’ils se comportent différemment – entre eux et par rapport à la souche virale originelle. Suite à des modifications accumulées dans leur ADN, ils peuvent se propager plus facilement, voir la gravité de la maladie qu’il provoque modifiée, etc. Grâce à leur propagation plus rapide, ils ont rapidement envahi le monde entier. Ce faisant, ils ont entraîné des augmentations fortes du nombre d’infections, appelées vagues épidémiques.
Si les modèles classiques sont incontournables, ils ont toutefois une limite : s’ils pouvaient prédire à quelle vitesse un nouveau variant allait remplacer une forme préexistante, ils n’avaient pas de moyen d’estimer l’amélioration de laquelle de ses capacités était en cause… Car en mutant, un virus peut devenir plus efficace de plusieurs façons différentes, liées à son mode de multiplication comme à son hôte – nous.
C’est là que le développement d’un nouveau type de modèle, comme celui que nous venons de publier, est précieux.
Force et vitesse : les deux capacités qui distinguent les variants
Le cycle de vie du SARS-CoV-2 peut être résumé ainsi : le virus infecte une personne et se réplique dans les cellules de son nasopharynx (nez et gorge). Au bout d’un ou deux jours, la personne infectée excrète des virus qui peuvent infecter ses contacts. Le pic de transmission se produit autour du cinquième jour après l’infection (pour les formes initiales du virus).
Au bout d’une dizaine de jours, la personne infectée ne libère plus de virus infectieux. C’est la fin de la « vie » du virus au sein de cet hôte… mais qu’en est-il de ses « descendants », tous les virus excrétés par l’ex-infecté ? S’ils ont atteint de nouveaux hôtes, ils vont provoquer des infections secondaires. Le nombre moyen de nouveaux cas provoqués par ces « descendants » constitue le nombre de reproduction effectif (Re, ou Rt) – parfois appelé « force » du virus.
Ce nombre était d’environ 3 au début de l’épidémie : chaque malade infectait à son tour trois contacts en moyenne. Ce chiffre a ensuite évolué au fil de l’épidémie, du fait des mesures de contrôle, le développement de l’immunité dans la population… et l’évolution des variants.
Mais la croissance d’une population virale est aussi déterminée par un second facteur : le temps de génération, en quelque sorte la « vitesse » du cycle viral, qui correspond à l’intervalle de temps entre l’infection initiale et une infection secondaire. Plus il est court, plus la propagation est rapide. Un virus qui infecte trois personnes en moyenne après deux jours se propagera beaucoup plus rapidement qu’un autre qui a besoin de cinq jours.
François Blanquart, Fourni par l’auteur
Les épidémiologistes ont soupçonné que ce temps de génération pouvait être raccourci pour les variants Alpha puis Delta par rapport aux 5 jours (en moyenne) des formes initiales, ce qui pourrait expliquer en partie leur succès. Mais les mesures du temps de génération sont délicates à mener, difficiles à comparer entre elles et ont donné des résultats contradictoires.
Des concepts bien connus en démographie… humaine
Les concepts de nombre de reproduction effectif et de temps de génération permettent de longue date de décrire la croissance de nombreuses espèces.
De la même façon que l’on peut prédire la croissance de la population virale en modélisant que chaque hôte infecté par le SARS-CoV-2 infecte environ trois personnes, entre deux et dix jours après l’infection (avec une moyenne à cinq jours), on peut décrire la croissance de la population humaine en supposant que chaque être humain laisse en moyenne deux descendants, entre 20 et 40 ans après sa naissance (avec une moyenne à 30 ans).
Ce type de modèles a été introduit en écologie dans les années 1950-1960 par LaMont Cole, alors professeur d’écologie à la Cornell University (États-Unis). Il s’intéressait à la diversité de cycles de vie des insectes, et se demandait pourquoi certains, comme la libellule, se reproduisaient une fois avant de mourir, tandis que d’autres, comme le moustique, se reproduisaient en continu. Ce qui l’amena à modéliser le nombre de descendants que pouvait avoir chaque espèce au cours de sa vie, et les avantages respectifs des stratégies adoptées.
Ces travaux précurseurs ont été généralisés dès 1965 par Richard Lewontin, un des biologistes des populations les plus importants du XXe siècle. En découlèrent des modèles très proches de ceux utilisés aujourd’hui pour décrire la propagation du SARS-CoV-2.
Les limites des modèles classiques
Mais revenons à nos variants… Leur croissance dépend, on l’a dit, de la vitesse de leur cycle de vie, ou temps de génération, et de leur force, soit le nombre moyen d’infections secondaires produites (nombre de reproduction effectif).
Le problème est que, avec les modèles classiques, les épidémiologistes suivent seulement la croissance de la population du variant, qui résulte à la fois de la vitesse et de la force du virus – et sans pouvoir distinguer ces deux composantes de façon simple.
Pourtant, pour comprendre et maîtriser les vagues épidémiques générées par des variants toujours différents, cette distinction est cruciale car les implications ne sont pas les mêmes.
La taille totale d’une vague dépend ainsi uniquement de la force du virus, et non de sa vitesse. En effet, la vague commence à refluer lorsqu’en moyenne le nombre de reproduction effectif passe sous le seuil de 1, c’est-à-dire que chaque individu infecté génère en moyenne moins d’une nouvelle infection – peu importe la vitesse du cycle de vie.
À cause de ce point aveugle, la plupart des études de modélisation supposaient que l’avantage de croissance des variants (par rapport aux souches circulant au préalable) était uniquement lié à une plus grande force du virus. Que chaque infection par un variant générait un plus grand nombre d’infections secondaires que ses prédécesseurs. Mais la communauté scientifique était bien consciente que cet avantage pouvait aussi être lié à une plus grande vitesse, donc un temps de génération plus court.
[Près de 80 000 lecteurs font confiance à la newsletter de The Conversation pour mieux comprendre les grands enjeux du monde. Abonnez-vous aujourd’hui]
Un nouveau modèle distinguant force et vitesse des variants
Pour remédier à ce problème, nous avons construit un modèle mathématique capable pour la première fois d’inférer comment vitesse et force d’un variant donné se combinent pour déterminer le taux de croissance de nouvelles souches virales.
La clé était de remarquer que, selon le nombre de contacts entre individus, l’avantage en termes de croissance du variant ne sera pas affecté de la même façon par sa vitesse et sa force :
-
Lorsqu’il y a de nombreux contacts entre individus, un « variant à grande vitesse », qui engendre rapidement de nouvelles infections, sera très avantagé.
-
Lorsqu’il y a moins de contacts, par exemple en cas de confinement, un variant à grande vitesse aura un avantage moindre.
-
Dans une situation où l’épidémie décroit (notamment du fait d’une diminution du nombre de contacts), il devient désavantageux d’avoir une grande vitesse, car cela ne fera qu’accélérer sa décroissance !
Ces résultats étaient déjà anticipés par Lewontin en 1965. Ils résultent d’une propriété mathématique intéressante des modèles démographiques, où la structure en âge d’une population reflète sa croissance. C’est un phénomène bien connu en démographie humaine, où les populations en croissance sont très jeunes, tandis que les populations en déclin comptent beaucoup de personnes âgées. Ainsi, dans une population en croissance, il est d’autant plus intéressant de se reproduire tôt (à grande vitesse) que les individus jeunes sont nombreux – créant comme une espèce d’emballement.
Dans le cas des virus et des hôtes infectés, l’« âge » est le temps depuis lequel un individu est infecté.
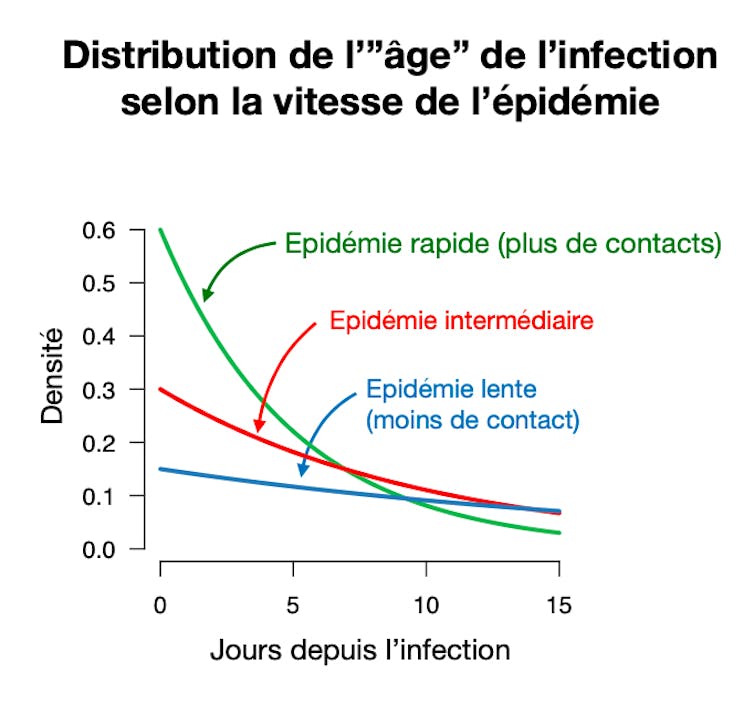
François Blanquart, Fourni par l’auteur
Quelles interprétations pour les différentes vagues de Covid ?
Pour le SARS-CoV-2, nos résultats impliquent que, si nous observons un variant quand des mesures de contrôle sont instaurées (port de masque, distanciation), il est possible d’examiner comment elles vont modifier son avantage de croissance par rapport aux lignées préexistantes. Et l’on peut déduire s’il a une plus grande vitesse ou une plus grande force.
C’est ce que nous avons fait, notamment dans le cadre de l’émergence et de la propagation du variant Alpha au Royaume-Uni en fin 2020-début 2021 – alors que des mesures de contrôle fortes avaient été mises en place. Nous avons inféré que son avantage de croissance ne diminuait que faiblement suite à ces mesures, et donc que son avantage était probablement lié à une plus grande force (un variant qui produit plus d’infections secondaires), plutôt qu’à une plus grande vitesse.
Plus précisément, nous avons estimé que le variant Alpha produisait +54 % d’infections secondaires par rapport aux souches précédentes. Et dans une seconde analyse, que Delta produisait lui-même +140 % d’infections secondaires par rapport à Alpha, avec des temps de génération comparables, ce qui renforce le résultat d’études épidémiologiques qui n’avaient trouvé que peu de différence.
Ces résultats établissent que temps de génération des infections secondaires et taux de transmission jouent tous deux un rôle important sur la croissance d’un virus et de ses variants.
Des perspectives importantes
Ce nouveau modèle mathématique pourra aider les épidémiologistes à mieux prédire la trajectoire des nouveaux variants de SARS-CoV-2 et à déterminer comment contrôler au mieux leur propagation.
Par exemple, une équipe britannique a inféré indépendamment, en utilisant une méthode analogue à la nôtre, que le variant Omicron avait une plus grande vitesse que son prédécesseur le variant Delta, ce qui semble confirmer les résultats d’études épidémiologiques sur la transmission intrafoyer.
Mais pour Omicron, ce n’est pas là toute l’histoire… Il est établi que ce variant a également tiré son avantage de sa très grande capacité à échapper au système immunitaire des hôtes vaccinés ou préalablement infectés. Il a ainsi la capacité de réinfecter des hôtes déjà immunisés par les vaccins et les vagues précédentes de SARS-CoV-2.
Nous pouvons spéculer que les variants touchent leurs limites en termes de vitesse et de force intrinsèques. Par exemple, si les variants Alpha et Delta ont augmenté leur force de +50 % et +140 % respectivement par rapport à la souche initiale, alors le nombre de reproduction de base de Delta serait de 11 – du même ordre de grandeur que pour le virus de la rougeole (entre 10 et 20), connu pour être très élevé. Pour faire encore « mieux », les nouveaux variants pourraient dériver l’essentiel de leur avantage de leur échappement au système immunitaire.
Nous travaillons d’ailleurs en ce moment à quantifier l’échappement au système immunitaire d’Omicron, en utilisant le « retard » de propagation du variant chez les non-vaccinés par rapport aux vaccinés. En effet, lorsque des mutations permettent à un variant de contourner le système immunitaire d’un hôte, il se propage déjà chez les vaccinés ou ceux qui ont été infectés précédemment… puis chez les autres.
Nous aurons ainsi des modèles et méthodes pour mieux comprendre les trois différentes stratégies qui avantagent les variants émergents – plus grande vitesse, plus grande force et échappement à l’immunité.
[the_ad id= »247816″]
CLIQUEZ ICI POUR LIRE PLUS SUR theconversation.com





GIPHY App Key not set. Please check settings